Fernanda Ramos, Sílvia Barros, Tiago Luís, Ana Margarida Henriques, Inês Maia Margarida Santos, Margarida Duarte
Unidade Estratégica de Investigação e Serviços em Produção e Saúde Animal, Instituto Nacional de Investigação Agrária e Veterinária
Os equinos representam um património de grande valor económico, cultural e desportivo, sendo fundamentais em múltiplos setores que vão desde a agricultura e o lazer até ao desporto de alta competição. As provas equestres, que se realizam em praticamente todos os continentes, assumem atualmente uma relevância global, não só pela sua dimensão económica e turística, mas também pelo prestígio cultural e desportivo que proporcionam. Neste contexto, é essencial realizar um controlo sanitário dos animais antes da sua movimentação para participarem em eventos equestres nacionais e internacionais, a fim de garantir a saúde dos equinos, salvaguardar a segurança dos animais participantes com os quais contactam, assegurar que não ocorram introduções de novos agentes nos países de destino e validar a credibilidade internacional das competições.
Assim, para um equídeo poder ser movimentado para fora das nossas fronteiras, é imprescindível o cumprimento de um conjunto de requisitos regulamentares:
- Detenção de um documento de identificação do equídeo (DIE)/Passaporte válido, documento oficial que identifica os animais nascidos em território nacional ou introduzidos em livre prática na União Europeia, constituindo um documento único, vitalício e obrigatório para todos os equídeos, emitido pela Direção-Geral de Alimentação e Veterinária (DGAV) ou pelos respetivos serviços regionais.
- Ausência de sinais clínicos de doenças infetocontagiosas, condição indispensável para garantir a segurança sanitária durante o transporte e a participação em eventos.
- Vacinação obrigatória contra influenza equina e tétano, medida preventiva essencial para reduzir o risco de disseminação destes agentes patogénicos.
- Detenção de certificados sanitários com resultados laboratoriais negativos, relativos a determinadas doenças, variando em função das exigências específicas do país de destino.
- Detenção de documentação de transporte emitida pela DGAV, contendo informação detalhada sobre a origem, o destino e a data/hora de partida do animal.
- Detenção de declarações oficiais sobre a inexistência de determinadas doenças no país de origem, aceites por alguns países como alternativa aos comprovativos das testagens laboratoriais negativas, desde que emitidas por autoridade competente.
Na União Europeia, a deslocação transfronteiriça de equídeos está sujeita a dois sistemas complementares de controlo sanitário: o TRACES (Trade Control and Expert System), que é uma plataforma informática de gestão e monitorização que assegura a rastreabilidade e o controlo oficial dos movimentos de animais e produtos de origem animal no espaço comunitário e o certificado sanitário (modelo 132 da DGAV), que é um documento oficial emitido pelas entidades descentralizadas da DGAV, que valida o cumprimento das exigências sanitárias nacionais e comunitárias para o transporte de equídeo.
Entre as medidas de controlo sanitário aplicadas a estas movimentações, a realização de testes laboratoriais prévios, destinados a confirmar que os animais estão em boas condições higieno-sanitárias e não estão infetados por agentes patogénicos de relevância epidemiológica, é uma exigência para assegurar que apenas animais saudáveis, e livres de agentes de risco, sejam autorizados a participar em competições e eventos equestres.
Os boletins de análise contendo os resultados laboratoriais são emitidos pelo Instituto Nacional de Investigação Agrária e Veterinária (INIAV, I.P.) que desempenha a função de Laboratório Nacional de Referência (LNR) para as doenças animais.
A DGAV, enquanto autoridade veterinária nacional, decide sobre a movimentação dos equídeos com base nos boletins laboratoriais e no cumprimento das restantes exigências anteriormente mencionadas. A emissão dos respetivos certificados sanitários obedece ao disposto no Regulamento (UE) 2016/429 do Parlamento Europeu e do Conselho, de 9 de março de 2016, relativo às doenças animais transmissíveis – conhecido como Lei da Saúde Animal – que altera e revoga diversos atos no domínio da saúde animal. Este enquadramento normativo inclui, em particular a Diretiva 2009/156/CE, de 30 de novembro de 2009, que estabelece as condições de polícia sanitária aplicáveis à circulação de equídeos e às importações provenientes de países terceiros.
As doenças virais são particularmente preocupantes na movimentação internacional de equídeos, devido ao seu elevado impacto clínico e elevada contagiosidade. No entanto, a exigência de apresentação de resultados laboratoriais negativos para determinadas infeções virais varia de acordo com a região geográfica e com as especificidades regulamentares de cada país.
A nível nacional e europeu, as seis doenças virais prioritárias, mais comumente requeridas para a movimentação de equídeos são a anemia infeciosa equina (AIE), a arterite viral equina (AVE), a rinopneumonia equina (EHV-1 e EHV-4), o exantema coital equino (EHV-3), a peste equina africana, e a influenza equina. Apenas estas patologias são abordadas neste artigo, dado o seu enquadramento regulamentar e sanitário.
Do ponto de vista epidemiológico, clínico e económico, cada uma destas doenças virais apresenta uma relevância distinta, sendo classificadas como doenças de declaração obrigatória ou de controlo oficial. Para outras doenças, como a estomatite vesicular ou as encefalomielites equinas (incluindo a febre do Nilo), podem ser exigidos certificados sanitários para animais provenientes de origens específicas, embora tal nunca tenha sido requerido a Portugal. No entanto, o INIAV está capacitado para o seu diagnóstico, garantindo conformidade com as exigências internacionais.
O presente artigo tem como objetivos:
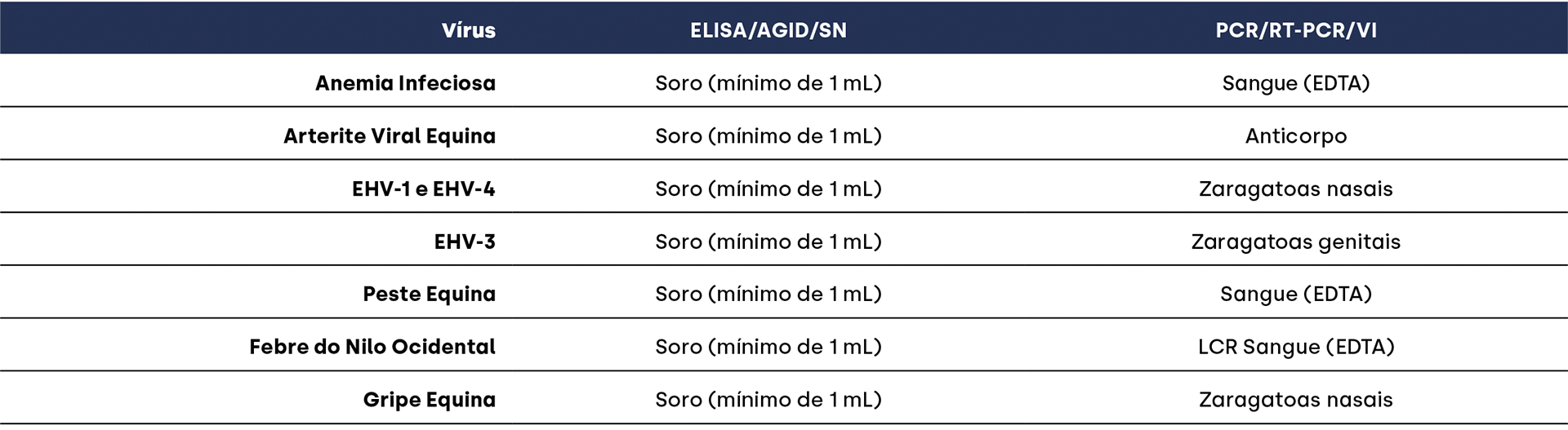
- Divulgar os métodos de diagnóstico serológico e virológico atualmente utilizados pelo LNR para a realização dos testes relativo às sete doenças virais prioritárias;
- Informar sobre os tipos de amostras biológicas que devem ser enviadas para a execução de cada um destes testes;
- Dar a conhecer os tempos de resposta disponibilizados pelo LNR;
- Sensibilizar criadores, treinadores, médicos veterinários e entidades organizadoras para a importância do cumprimento destas medidas, de modo a garantir a participação responsável dos equídeos em competições e eventos equestres, em conformidade com a legislação vigente e com as boas práticas de sanidade animal.
1. Anemia Infeciosa Equina (AIE)
1.1. A doença
A Anemia Infeciosa Equina (AIE) é causada por um retrovírus do género Lentivirus. A transmissão ocorre predominantemente de forma mecânica, através de insetos hematófagos, bem como por agulhas ou instrumentos contaminados. A infeção apresenta-se, na maioria dos casos, sob forma crónica, manifestando-se por febre, anemia e emagrecimento progressivo, sendo que os animais permanecem portadores durante toda a vida. Na fase aguda, a doença é caracterizada por icterícia, depressão, febre, perda de peso e edemas generalizados. No entanto, muitos animais não apresentam sinais clínicos evidentes, mas são portadores da doença, continuando a transmitir o vírus, já que não existe cura. Não há vacinas disponíveis para a AIE.
A AIE é uma doença de declaração obrigatória, reconhecida tanto pela Organização Mundial de Saúde Animal (WOAH) como pela União Europeia.
1.2. O diagnóstico
O diagnóstico serológico baseia-se na deteção de anticorpos que traduzem geralmente o contacto com o vírus, já que não existe vacina. O teste de Coggins (agar gel immunodiffusion-AGID) é considerado o método de referência, pela sua elevada especificidade e simplicidade de execução. O teste baseia-se na formação de linhas de precipitação de imunocomplexos quando os anticorpos presentes no soro, reagem com antigénio específico.
A técnica ELISA (Enzyme-Linked Immunosorbent Assay) pode ser utilizada como técnica complementar de rastreio, permitindo a identificação mais rápida de animais potencialmente infetados. No entanto, como apresenta menor especificidade levando à ocorrência de resultados falso-positivos, os resultados positivos devem ser confirmados posteriormente pelo teste de Coggins.
Em potros com idade até aos 6 meses em amamentação, pode ocorrer um resultado positivo na pesquisa de anticorpos, devido à presença de anticorpos de origem materna adquiridos pela ingestão de colostro. Nestes casos, a prova deve ser repetida mais tarde para confirmação ou exclusão da possível infeção.
A deteção de RNA viral é feita muito esporadicamente por RT-PCR em amostras de sangue não coagulado, tendo como alvo o gene gag1.
2. Arterite Viral Equina (AVE)
2.1. A doença
A Arterite Viral Equina (AVE) é causada por um vírus pertencente ao género Alphaarterivirus, da família Arteriviridae. A transmissão ocorre principalmente por via respiratória e venérea, neste caso, através de garanhões portadores que excretam o vírus no sémen.
A maioria das infeções permanece subclínica, passando frequentemente despercebida. Quando os sinais clínicos estão presentes, estes podem variar em forma e gravidade, caracterizando-se principalmente por episódios de febre, depressão, anorexia, edema (especialmente nos membros, escroto e prepúcio nos garanhões), conjuntivite e reação cutânea do tipo urticária2.
Para além dos casos de aborto em éguas gestantes e da mortalidade observada em potros jovens, associada a pneumonia intersticial fulminante, enterite ou pneumo-enterite, a taxa de mortalidade em surtos de AVE é geralmente baixa, verificando-se que os animais afetados recuperam completamente. No entanto, uma percentagem variável de garanhões infetados, podem tornar-se portadores crónicos, eliminando o vírus pelo sémen e constituindo, assim, uma fonte persistente de disseminação da infeção.
Existem vacinas para a Arterite Viral Equina (AVE), geralmente com vírus inativado, que ajudam a prevenir abortos em éguas e a disseminação do vírus em garanhões, mas em Portugal não é praticada.
A AVE é uma doença de declaração obrigatória a nível europeu e internacional, exigindo a implementação de medidas rigorosas de vigilância e controlo sanitário.
2.2. O diagnóstico
O diagnóstico baseia-se em testes serológicos, nomeadamente a seroneutralização (SN) e a ELISA, complementados pela deteção do genoma viral por métodos moleculares (RT-PCR), realizados em amostras de soro ou sémen, respetivamente.
O teste de seroneutralização é o método de referência recomendado pela WOAH. Neste ensaio células susceptíveis são inoculadas com vírus padrão que foi previamente incubado com diluições seriadas dos soros a testar. A presença de anticorpos neutralizantes específicos resulta na inibição da atividade viral, prevenindo a ocorrência de lise celular e confirmando a resposta imunitária contra o vírus. Este método permite a quantificação dos anticorpos presentes no soro, que é calculada pelo método de Spearman-Kärber2. A presença de anticorpos é indicativa de doença em animais não vacinados.
A deteção de genoma viral é feita por RT-PCR utilizando um sistema dirigido para o gene N (nucleocapsid protein, ORF 7).
3. Rinopneumonia dos Equinos (Herpesvírus dos tipos EHV-1 e EHV-4)
3.1. A doença
A rinopneumonia equina (RPE) designa qualquer uma das doenças clínicas contagiosas dos equídeos que podem ocorrer como resultado da infeção por herpesvírus equino-1 (EHV-1) ou por herpesvírus equino-4 (EHV-4), dois vírus geneticamente relacionados. A infeção pelo EHV-1 está listada pela WOAH como sendo de declaração obrigatória. A infeção primária por estes dois vírus é caracterizada por patologia do trato respiratório superior de gravidade variável, dependendo da idade e do estado imunológico do animal afetado. O EHV-1 pode causar complicações mais graves, nomeadamente aborto, morte perinatal do potro ou doença neurológica. O EHV-4 tem sido associado a casos esporádicos de aborto, mas não está associado a grandes surtos, como o que se pode verificar com o EHV-1.
Tal como para outros herpesvírus, o EHV-1 e o EHV-4 induzem infeções latentes, e o vírus permanece em fase de latência no gânglio trigeminal e em tecidos linfoides (linfonodos e baço). Ensaios de infeção experimental com EHV-1, mostraram que, após a fase aguda caracterizada por febre, excreção nasal e virémia, o vírus deixa de ser detetável em secreções, mas permanece no gânglio trigeminal, de onde pode reativar futuramente 3. A reativação pode ocorrer em situações de stress (transporte, maneio, doenças concomitantes, gestação), levando a nova excreção nasal e, no caso de EHV‑1, potencialmente a abortos ou ao aparecimento de sinais neurológicos.
Os vírus EHV-1 e EHV-4 são endémicos na maioria das populações equinas domésticas em todo o mundo. A maioria dos cavalos é suscetível de ser reinfectada várias vezes durante a sua vida, muitas vezes de forma ligeira ou subclínica.
A transmissão ocorre por contacto direto entre animais, através de secreções respiratórias ou indiretamente, através de contacto com equipamentos contaminados. Estes vírus apresentam elevada importância sanitária pela sua rápida disseminação em efetivos equestres e pelo impacto económico e desportivo dos surtos. Embora não sejam atualmente de declaração obrigatória à Comissão Europeia, vários países mantêm programas de vigilância e notificação voluntária 4,5.
3.2. O diagnóstico
O diagnóstico é realizado através de testes moleculares (PCR) e serológicos (ELISA).
O método molecular utlizado para deteção de genoma viral é o recomendado pela WOAH, e assenta num sistema duplex de PCR em tempo real (qPCR). Este sistema utiliza dois pares de primers e duas sondas dirigidos respetivamente para o gene da glicoproteína gB e à ORF17 que codifica a proteína UL43 (https://www.woah.org/fileadmin/Home/eng/Health_standards/tahm/2.05.09_EQUINE_RHINO.pdf). Nos ensaios de qPCR, cargas virais elevadas traduzem‑se em valores de Ct reduzidos (cycle threshold, ciclo a partir do qual a emissão de luz é detetável pelo sistema), enquanto as amostras com baixa carga viral apresentam valores de Ct mais elevados. O valor de Ct é portanto inversamente proporcional à quantidade de material genético inicial presente na amostra.
As amostras mais comumente utilizadas para a realização do ensaio incluem zaragatoas oro-nasais ou amostras de sangue. A interpretação de um resultado de qPCR negativo não exclui latência, apenas indica ausência de excreção viral ou virémia detetável no momento da colheita. Por outro lado, um resultado positivo deve ser interpretado em função do tipo de amostra6. Em secreções respiratórias (recolhidas por zaragatoas oro‑nasais), um qPCR positivo com valor de Ct baixo (carga viral elevada) na presença de sinais respiratórios sugere forte evidência de infeção ativa/excreção, tanto para EHV‑1 como EHV‑4. Um qPCR positivo com valor de Ct alto (carga viral baixa) em animal assintomático pode indicar uma excreção viral mínima, uma infeção recente em fase de resolução ou reativação subclínica, com baixo risco de transmissão do vírus.
Em amostras de sangue (com EDTA), um qPCR positivo é indicativo de virémia, tipicamente associada à fase aguda ou à reativação viral com disseminação sistémica, especialmente no caso de EHV‑1. Isto é relevante em contexto de risco de aborto e de doença neurológica.
Um qPCR negativo em sangue, mas positivo em secreções respiratórias, sugere infeção localizada ao trato respiratório. Um qPCR negativo em sangue e nas secreções, mas positivo em tecidos nervosos/linfoides (recolhidos pós‑morte ou por biópsias específicas) é compatível com fase de latência, sobretudo quando associada a ausência de sinais clínicos significativos.
Em conclusão, a realização de qPCR em zaragatoas oro‑nasais e/ou em amostras de sangue permite detetar infeção ativa, excreção viral e virémia, mas não possibilita a identificação direta de animais em estado de latência. Um resultado negativo não exclui a presença de infeção latente, enquanto um resultado positivo com carga viral muito baixa pode refletir a deteção de genoma residual ou uma reativação subclínica.
4. Exantema Coital (EHV3)
4.1. A doença
O exantema coital equino é uma doença mucocutânea altamente contagiosa, embora geralmente benigna, que afeta sobretudo equídeos utilizados na de reprodução e que se transmite predominantemente por via sexual. Caracteriza-se pela formação de pápulas, vesículas, pústulas e úlceras nos órgãos genitais externos de éguas e garanhões. Esta infeção é causada por um alphaherpesvirus, Equid alphaherpesvirus 3 (EHV‑3), pertencente à família Herpesviridae. A doença é endémica a nível mundial, sendo o vírus transmitido por contacto direto durante o coito e por intermédio de instrumentos contaminados utilizados em procedimentos reprodutivos. O EHV‑3 replica principalmente no epitélio genital, não sendo geralmente, um vírus invasivo ou sistémico. Assim, a doença não envolve outros órgãos e, embora não cause infertilidade ou aborto, tem um impacto negativo na indústria equina, uma vez que obriga à suspensão temporária da atividade reprodutiva dos animais infetados. Tal como para outros herpesvírus, o EHV‑3 é capaz de estabelecer latência, nomeadamente em gânglios sensoriais (por exemplo, no gânglio sacral), com possibilidade de reativação periódica, sobretudo em situações de stress ou de atividade reprodutiva intensiva. Animais sem lesões aparentes podem, por conseguinte, voltar a excretar o vírus, constituindo fonte de infeção para parceiros de cobrição 7.
Atualmente não existe uma vacina comercialmente disponível para o EHV-3, pelo que o controlo da doença assenta no repouso sexual, e na aplicação de práticas de biossegurança em centros de reprodução e na implementação rigorosa de medidas de sanidade e na aplicação de práticas de biossegurança em centros de reprodução.
4.2. O diagnóstico
O diagnóstico baseia‑se na observação de sinais clínicos característicos e confirmação laboratorial por PCR/qPCR.
A deteção de EHV-3 é efetuada no INIAV por um sistema de PCR em tempo real (qPCR), que utiliza um par de primers e uma sonda dirigidos para o gene da glicoproteína gG 8. Um resultado positivo revela a presença do vírus e a infeção.
5. Peste Equina Africana
5.1. A doença
A Peste Equina Africana (AHS) é uma doença altamente infeciosa e frequentemente fatal, que afeta todos os equídeos, sendo os cavalos a espécie mais suscetível. É causada pelo vírus da peste equina africana (AHSV), um Orbivirus pertencente à família Sedoreoviridae, estando atualmente reconhecidos nove serotipos distintos. A doença não é contagiosa por contacto direto, sendo a transmissão realizada principalmente através da picada de insetos hematófagos do género Culicoides.
A doença caracteriza-se por alterações graves das funções respiratória e circulatória. Na forma respiratória aguda, os animais afetados apresentam febre alta, edema pulmonar acentuado, dispneia, tosse e descarga nasal abundante. Na forma cardíaca, observam-se edemas nas pálpebras, lábios e pescoço. A forma mista combina manifestações das duas apresentações anteriores, manifestando-se inicialmente por sinais respiratórios ligeiros, seguidos dos edemas característicos da forma cardíaca.
A doença é endémica na África subsaariana As zebras constituem o reservatório natural do vírus e raramente desenvolvem sinais clínicos 9. Foi ainda descrito que cães podem desenvolver doença grave após ingestão de carne de equinos infetados 10.
Portugal registou um episódio significativo de Peste Equina Africana no final da década de 1980. A doença foi identificada pela primeira vez no país no outono de 1989, na sequência de surtos previamente ocorridos em Espanha. Estes focos foram rapidamente controlados mediante a implementação de programas de vacinação massiva e medidas sanitárias rigorosas. Desde então, o país permanece livre da doença. No entanto, há vários anos que o INIAV participa em testes de proficiência internacionais, organizados pelo Laboratório de Referência Europeu (Madrid, Espanha) com o objetivo de avaliar e assegurar a capacidade técnica e a robustez laboratorial dos métodos de diagnóstico recomendados.
5.2. O diagnóstico
O diagnóstico é efetuado através de métodos moleculares (RT‑qPCR) e serológicos (ELISA). A técnica de ELISA utilizada baseia‑se na deteção de anticorpos dirigidos contra a proteína viral VP7, a qual se encontra conservada entre os diferentes serotipos. Dado que o país se encontra oficialmente livre da infeção, a DGAV não autoriza a vacinação do efetivo nacional, logo um resultado positivo na ELISA é interpretado como indicativo de infeção. Este resultado não permite, no entanto, determinar se o animal apresenta doença ativa no momento da colheita, se está virémico, ou se é infecioso para vetores Culicoides. Contudo esta informação pode ser obtida pela testagem de sangue (com EDTA) por RT-qPCR. O método utilizado no INIAV para deteção de RNA viral é o recomendado pelo EURL e é dirigido para o gene vp711.Um resultado positivo traduz a presença de RNA viral, revelando a presença AHSV nas amostras testadas.
6. Gripe Equina
6.1. A doença
A gripe equina é uma doença respiratória viral altamente contagiosa dos equídeos, causada pelo vírus influenza A. Esta infeção constitui uma das principais causas de doença respiratória em cavalos, caracterizando-se por elevada morbilidade e rápida disseminação em populações suscetíveis. Devido à sua importância sanitária e ao impacto económico associado, a gripe equina encontra-se classificada pela Organização Mundial da Saúde Animal (WOAH) como doença de declaração obrigatória.
A infeção manifesta-se predominantemente sob a forma de doença do trato respiratório superior, com início agudo e sinais clínicos que incluem febre, tosse seca, descarga nasal serosa a mucopurulenta, letargia e diminuição do desempenho atlético. A severidade do quadro clínico é influenciada por fatores como a idade, o estado imunológico e o estatuto vacinal dos animais afetados. Embora a mortalidade seja geralmente baixa, podem ocorrer complicações, nomeadamente infeções bacterianas secundárias, que prolongam o período de convalescença e agravam o impacto clínico e económico da doença.
O vírus da gripe equina apresenta elevada variabilidade genética, associada a fenómenos de drift e shift antigénicos, que contribuem para a emergência de novas estirpes e para a ocorrência de surtos em populações parcialmente imunizadas.
A transmissão do vírus da gripe equina ocorre predominantemente por via aerógena, através da inalação de aerossóis produzidos por animais clinicamente afetados. Pode também ocorrer transmissão indireta por contacto com superfícies contaminadas, o que se torna particularmente relevante na disseminação do agente em contextos de elevada densidade animal, como centros hípicos, eventos desportivos e instalações de treino.
O vírus da gripe equina é considerado endémico em numerosas populações equinas a nível global, sendo a maioria dos cavalos suscetível à infeção ao longo da vida, especialmente na ausência de programas vacinais adequados. Dada a elevada contagiosidade do agente, a sua capacidade de rápida disseminação e o impacto significativo no bem-estar animal e na indústria equina, a implementação de estratégias eficazes de vigilância epidemiológica, vacinação e biossegurança é fundamental para o controlo e prevenção da doença 12.
6.2. O diagnóstico
O diagnóstico é realizado através de testes moleculares (PCR) e serológicos (ELISA).
O método molecular para deteção de genoma viral é o mesmo utilizado em análises de rotina para a pesquisa de gripe aviária e baseia-se num sistema de RT-PCR em tempo real (RT-qPCR). Este sistema utiliza um par de primers e uma sonda dirigidos para o gene da matriz 13, um gene altamente conservado em todos os vírus do género Influenza A. As amostras mais adequadas para a realização do ensaio são zaragatoas nasais.
O diagnóstico serológico é efetuado através de um método comercial que se baseia na deteção de anticorpos dirigidos contra nucleoproteína, que se encontra conservada entre os diferentes vírus do género Influenza A, pelo que o mesmo método pode ser utilizado para a deteção de anticorpos contra este vírus tanto em soros de aves, como de suínos ou de equinos.
7. Casuística no Laboratório Nacional de Referência (2020-2025 (nov))
Entre 2020 e 30 de novembro de 2025 foram efetuados 1596 testes para fins de movimentação e/ou controlo sanitário (FNO) de equinos.
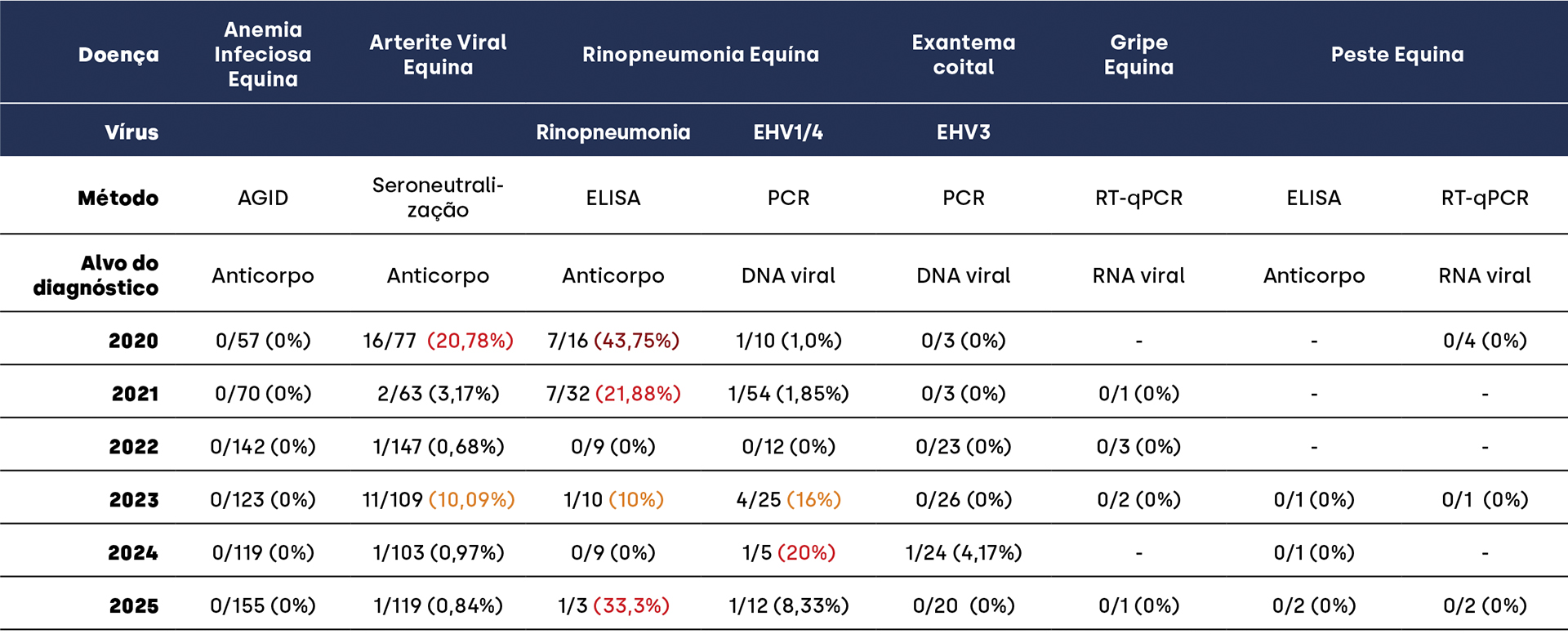
Tabela 1. Testes virológicos solicitados ao INIAV I.P. entre 2020 e 2025, no âmbito da movimentação de equinos.
Anemia Infeciosa equina
Os 664 equinos testados por AGID no período em análise foram negativos, corroborando a ausência de circulação da AIE em Portugal, em consonância com o estatuto sanitário oficialmente reconhecido do país. Na Europa, a AIE apresenta uma distribuição heterogénea, estando praticamente ausente ou sob controlo rigoroso na maioria dos países da Europa Ocidental e do Norte. Em algumas regiões da Europa de Leste a doença ocorre em focos endémicos. Assim, os resultados nacionais estão alinhados com o panorama da Europa Ocidental.
A AIE mantém-se endémica em várias regiões da Ásia, África e América do Sul, em consequência de fragilidades nos sistemas de vigilância, controlo de movimentos e práticas de biossegurança.
Arterite viral equina
Entre 2020 e 2025, dos 618 testes realizados para deteção de anticorpos específicos para AVE, foram consistentemente detetados soros positivos por seroneutralização, observando-se maior percentagem de positividade em 2020 (20,78%) e em 2023 (10,09%). Estes dados demonstram a circulação do vírus em Portugal ao longo do período analisado, uma vez que a vacinação contra a AVE não é praticada no país, pelo que a seropositividade reflete exposição natural ao vírus.
Este cenário é semelhante ao observado em vários países europeus, onde a AVE é considerada endémica, mas de baixa prevalência, com circulação silenciosa, frequentemente associada a garanhões portadores persistentes. A nível mundial, a AVE encontra-se amplamente distribuída, verificando-se surtos esporádicos na Europa, América do Norte e Ásia, sendo a vigilância baseada sobretudo em serologia e controlo reprodutivo.
Rinopneumonia dos Equinos (EHV-1 e EHV-4)
Embora o número de amostras testadas para anticorpos contra estes dois vírus tenha sido muito reduzido, os resultados serológicos por ELISA para EHV-1 e EHV-4 mostram valores de seroprevalência anuais variaram entre 21,88% e 43,75%. Estes valores indicam contacto prévio significativo das populações equinas com estes vírus, ou, em alguns casos, a presença de anticorpos vacinais quando a vacinação é praticada.
Na Europa, estudos epidemiológicos baseados em resultados em deteção de anticorpos revelam frequentemente seroprevalências elevadas, muitas vezes superiores a 60–80% em animais adultos, revelando a ampla disseminação destes herpesvírus. Assim, os valores observados em Portugal são compatíveis com uma circulação endémica, embora aparentem situar-se num intervalo inferior ao descrito nalguns países europeus.
Relativamente ao diagnóstico molecular, dos 118 equinos testados por PCR específico para EHV-1/EHV-4, 8 foram positivos (6,78%), com valores mais elevados em 2023 e 2024. Estes resultados estão de acordo com o conhecimento atual da epidemiologia dos EHVs, caracterizada por infeções persistentes e reativações intermitentes.
Exantema Coital (EHV3)
No período em análise, foram testados 99 equinos para Exantema Coital Equino, tendo sido identificado apenas um animal positivo em 2024, não havendo evidência de disseminação da infeção nem de ligação a surtos reprodutivos.
Na Europa e no mundo, esta doença é geralmente esporádica, estando associada a contextos reprodutivos específicos e ao uso de animais portadores assintomáticos, sendo, por isso, raramente detetada fora de programas de vigilância dirigida.
O número de amostras testadas para Gripe Equina e Peste Equina Africana foi extremamente reduzido, não tendo sido detetados animais positivos em concordância com a ausência de circulação da Peste Equina Africana na Europa e com a situação endémica controlada da Gripe Equina, cuja vigilância depende fortemente de sistemas de notificação clínica e de vacinação dos animais.
A testagem para Peste Equina foi realizada no âmbito de suspeita clínica e não para efeitos de movimentação animal. Uma vez que o país e a Europa estão livres da peste equina, a exigência de certificado sanitário a atestar a ausência de infeção não é solicitado pela maioria dos países destinatários.
8. Materiais para testagem de equinos em movimentação e recomendações de colheita e envio
A qualidade do diagnóstico virológico depende da adequação das amostras colhidas e da sua condição de preservação. Os métodos serológicos de ELISA, AGID e seroneutralização requerem soro do animal a testar, obtido a partir de amostra de sangue periférico. O sangue é colhido para tubo seco e deixado em repouso durante 15-20 minutos para favorecer o processo de coagulação. Deve então ser colocado no frio (frigorifico, 4-8ºC) durante algumas horas para promover a retração do coagulo e facilitar a separação do soro.
Para isolamento de vírus ou testagem molecular devem ser enviadas zaragatoas, sangue ou líquido cefalorraquidiano (LCR), consoante a pesquisa a efetuar (Tabela 2).
As zaragatoas devem ser enviadas secas (sem meio de cultura), conservadas no frio.
Para PCR/RT-PCR o sangue deve ser colhido para EDTA, sendo muito importante que o tubo seja imediatamente invertido duas ou três vezes para garantir que não haja coagulação em parte da amostra, o que dificulta os procedimentos laboratoriais.
As amostras devem ser refrigeradas imediatamente após a colheita. O correto acondicionamento e transporte das amostras é crucial para preservar a integridade do material genético viral e garantir a viabilidade de eventuais isolamentos virais em culturas celulares.
Todos os materiais biológicos devem ser sempre enviados no frio (por exemplo junto a um acumulador de frio) acompanhados de folha oficial de requisição de análises do INIAV (descarregável através do link https://www.iniav.pt/images/Servicos-Laboratoriais/saude-animal/Mod_GIC_019_FRA_Animais_exceto_canideos_e_felideos.pdf), corretamente preenchida.
O envio das amostras deve ser atempado, uma vez que, em algumas situações particulares, pode haver necessidade de repetir os testes.
9. Tempos de resposta do INIAV I.P.
Os prazos para obtenção de resultados laboratoriais variam conforme a complexidade das análises requeridas e a urgência da situação (ex. suspeita clínica de doença exótica).
O tempo máximo de resposta previsto para cada um destes testes serológicos e virológicos efetuados no Laboratório de Virologia da Unidade de Saúde Animal do INIAV, é o apresentado na Tabela 2, podendo, no entanto, variar em função do número de amostras rececionadas, do número de ensaios requeridos ou da necessidade de se realizar ensaios complementares subsequentes para esclarecer dúvidas, como por exemplo caraterização molecular por sequenciação. Depende ainda do stock de reagentes disponíveis, que caso entre em rotura por situações extraordinárias comprometerá a testagem. Neste caso, o cliente é notificado através do Gabinete de Informação ao Cliente (GIC).
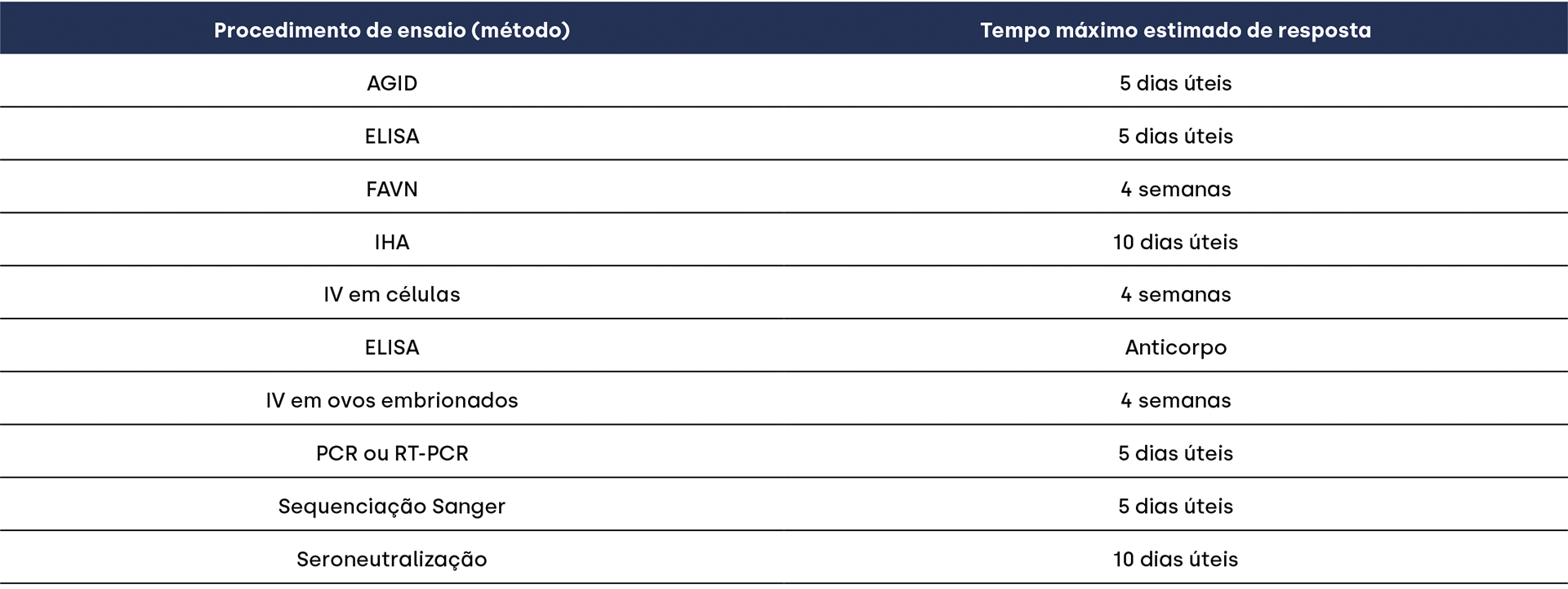
Tabela 3. Tempo máximo de resposta dos diferentes ensaios realizados no Laboratório de Virologia da UEISPSA do INIAV I.P.
Em casos de extrema urgência na resposta, como é uma suspeita clínica de doença inexistente no território, é possível obter resultados moleculares ao fim de 3-4 horas após a entrada do material. Este tempo compreende a extração automática de ácidos nucleicos e a reação de PCR/RT-PCR em tempo real. Também neste caso, o tempo necessário para a preparação do material varia exponencialmente com o número de amostras.
Em situações não urgentes, e para otimização de recursos, é realizado um procedimento de extração de ácidos nucleicos diário, pelo que se uma amostra chegar ao laboratório após a realização desse procedimento, será extraída no dia seguinte e o resultado poderá ser emitido para o cliente dentro de 24 a 120 horas.
Bibliografia
- Cook RF, Cook SJ, Li F, Montelaro RC, Issel CJ. Development of a multiplex real-time reverse transcriptase-polymerase chain reaction for equine infectious anemia virus (EIAV). Journal of Virological Methods. agosto de 2002;105(1):171–9.
- OIE Terrestrial Manual Chapter 3.5.10. Equine Viral Arteritis. Em.
- Slater JD, Borchers K, Thackray AM, Field HJ. The trigeminal ganglion is a location for equine herpesvirus 1 latency and reactivation in the horse. Journal of General Virology. 1 de agosto de 1994;75(8):2007–16.
- Khan MZ, Ji Y, Fan X, Liu Y, Liu W, Wang C. Equine Herpesvirus Infections: Treatment Progress and Challenges in Horses and Donkeys. Veterinary Sciences. 13 de novembro de 2025;12(11):1082.
- Liu D, Zhao X, Wang X. The Genomic Characterization of Equid Alphaherpesviruses: Structure, Function, and Genetic Similarity. Veterinary Sciences. 3 de março de 2025;12(3):228.
- Giessler KS, Samoilowa S, Soboll Hussey G, Kiupel M, Matiasek K, Sledge DG, et al. Viral Load and Cell Tropism During Early Latent Equid Herpesvirus 1 Infection Differ Over Time in Lymphoid and Neural Tissue Samples From Experimentally Infected Horses. Front Vet Sci. 4 de setembro de 2020;7:621.
- Vissani MA, Damiani AM, Barrandeguy ME. Equine Coital Exanthema: New Insights on the Knowledge and Leading Perspectives for Treatment and Prevention. Pathogens. 20 de agosto de 2021;10(8):1055.
- Vissani MA, Tordoya MS, Tsai YL, Lee PYA, Shen YH, Lee FC, et al. On-site detection of equid alphaherpesvirus 3 in perineal and genital swabs of mares and stallions. Journal of Virological Methods. julho de 2018;257:29–32.
- Porphyre T, Grewar JD. Assessing the potential of plains zebra to maintain African horse sickness in the Western Cape Province, South Africa. Simuunza MC, editor. PLoS ONE. 31 de outubro de 2019;14(10):e0222366.
- Hanekom J, Lubisi BA, Leisewitz A, Guthrie A, Fosgate GT. The seroprevalence of African horse sickness virus, and risk factors to exposure, in domestic dogs in Tshwane, South Africa. Preventive Veterinary Medicine. abril de 2023;213:105868.
- Agüero M, Gómez-Tejedor C, Angeles Cubillo M, Rubio C, Romero E, Jiménez-Clavero A. Real-time fluorogenic reverse transcription polymerase chain reaction assay for detection of African horse sickness virus. J Vet Diagn Invest. maio de 2008;20(3):325–8.
- Branda F, Yon DK, Albanese M, Binetti E, Giovanetti M, Ciccozzi A, et al. Equine Influenza: Epidemiology, Pathogenesis, and Strategies for Prevention and Control. Viruses. 21 de fevereiro de 2025;17(3):302.
- Spackman E, Senne DA, Myers TJ, Bulaga LL, Garber LP, Perdue ML, et al. Development of a real-time reverse transcriptase PCR assay for type A influenza virus and the avian H5 and H7 hemagglutinin subtypes. J Clin Microbiol. setembro de 2002;40(9):3256–60.

 ©iStock
©iStock